

自2019年底第一例新冠阳性病例确诊以来,SARS-CoV-2病毒已经在全球造成了超过4亿人次的感染。SARS-CoV-2病毒的刺突(S)蛋白介导病毒与宿主细胞表面的ACE2受体结合,是抗SARS-CoV-2病毒抗体药物开发的理想靶标。S蛋白与 ACE2结合的关键区域被称为RBD区域,使用中和抗体阻断RBD与ACE2的结合可有效阻止SARS-CoV-2病毒感染。然而,由于SARS-CoV-2是单链病毒,非常容易突变,目前已有许多突变毒株的产生,抗体的广泛中和能力也是一个重要的考量因素。
在新冠疫情发生后,细胞工程及抗体药物教育部工程研究中心朱建伟教授团队与国内外多家企事业单位合作,从康复患者B细胞中克隆并筛选得到了多个对SARS-CoV-2病毒具有强效中和作用的抗体。在经过一系列的体内体外活性评价、抗体作用机制研究、结构解析、安全性评价、成药性评价和生产工艺开发后,该团队成功获得了最具开发价值的候选抗体2G1,目前该抗体已经获得临床批件。相关成果近日发表在著名期刊Cell Discovery上。
该研究首先采集了新冠康复患者的血液样本,从中分离得到了记忆B细胞,然后克隆得到了数百个IgG抗体分子。通过一系列的结合能力筛选以及假病毒中和实验筛选,最后得到了数十个候选抗体(图1)。在这些候选抗体中,2G1表现出了最强的中和活性,因此对其做了进一步评价。
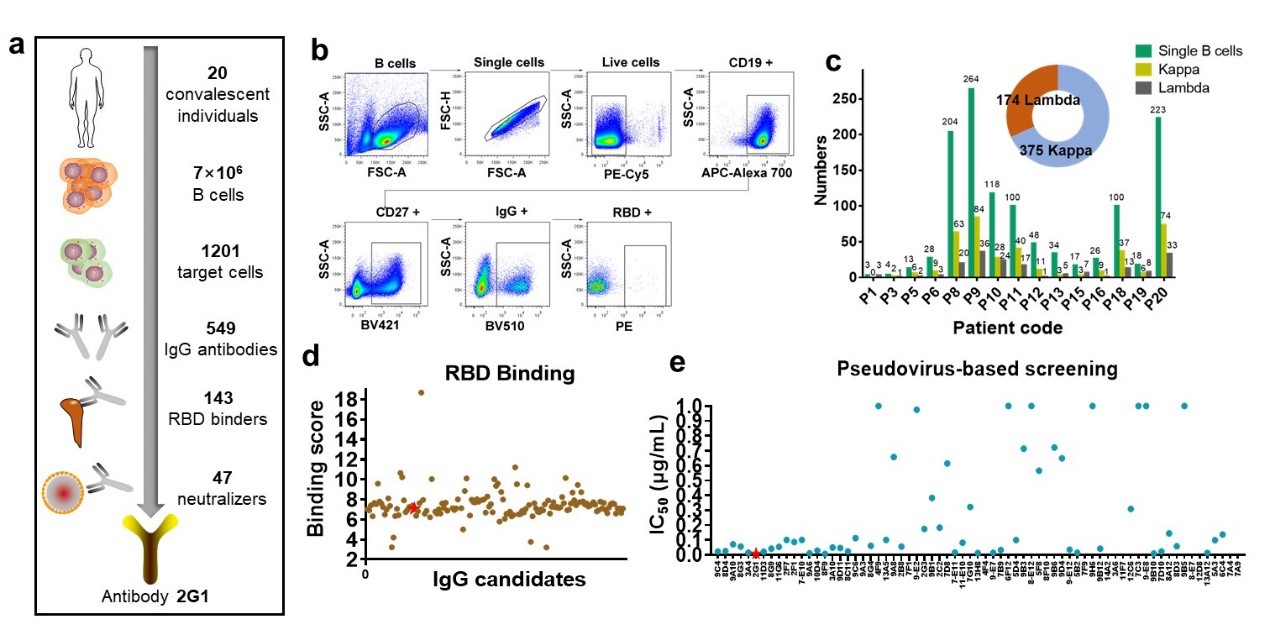 图1. SARS-CoV-2中和抗体开发流程
图1. SARS-CoV-2中和抗体开发流程
随后研究团队探索了一些主要突变位点和主要突变毒株对抗体2G1活性的影响,发现N439K、Y453F、E484K和N501Y等突变位点以及Alpha、Beta、Gamma和Delta等引起担忧的毒株均对2G1的活性不构成显著影响(图2)。抗体2G1与主要突变毒株具有纳摩尔级的亲和力。这表明抗体2G1抗突变能力良好,对SARS-CoV-2具有广泛的中和能力。
 图2. 抗体2G1的抗突变能力评价
图2. 抗体2G1的抗突变能力评价
该研究同时使用转基因小鼠模型和恒河猴模型评价了抗体2G1的体内活性。在转基因小鼠实验中,使用20、6.7或2.2 mg/kg剂量的2G1均可以完全保护小鼠免受WA1/2020毒株和Beta毒株的感染,2G1保护小鼠免受Delta毒株感染的剂量在6.7 - 20 mg/kg之间。基于恒河猴的实验也得到了相似的结果,这进一步肯定了2G1的高效中和能力。
冷冻电镜的结构解析结果表明,抗体2G1通过广泛的疏水作用结合到了S蛋白三聚体的尖端区域,与S蛋白的结合面积非常小,避开了大多数的突变位点,这是其具有广泛抗突变能力的原因(图3)。多个抗体的组合是对抗SARS-CoV-2病毒变异的有效手段,较小的接触面积使得2G1不会轻易与其他抗体产生表位冲突,因此具有较高的联用价值。
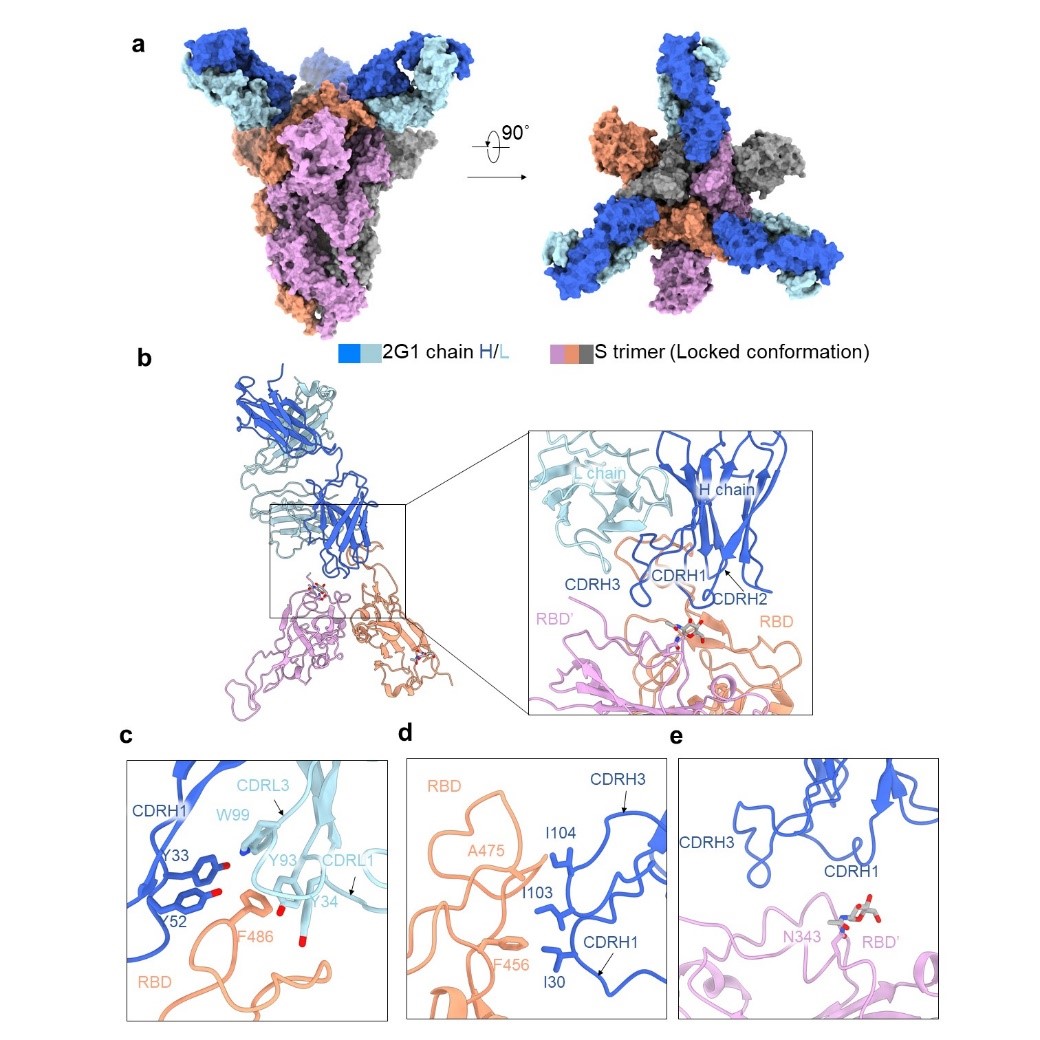 图3. 抗体2G1的表位解析
图3. 抗体2G1的表位解析
该项研究通过B细胞克隆技术,筛选得到了系列有价值的SARS-CoV-2中和抗体,对新冠感染的治疗和新冠疫情的控制具有非常积极的意义。文章的第一通讯作者是8188www威尼斯朱建伟教授,博士研究生马航和唐浩能为共同第一作者。西湖大学周强教授等多位合作者为该研究提供了帮助。
全文链接:
https://www.nature.com/articles/s41421-022-00381-7