
学科科研

学科科研
阿尔茨海默病(AD)是一种中枢神经系统退行性疾病,病理主要表现为脑内β淀粉样蛋白(Aβ)沉积形成的神经炎性斑块,异常过度磷酸化tau蛋白聚集形成的神经纤维缠结,以及广泛存在的中枢神经炎症反应。近几十年来AD疾病修饰类药物研发多以Aβ为主要靶标,但迄今为止只有两种Aβ抗体药物(Aducanumab和Lecanemab)获得了FDA批准,其中Aducanumab已经基本退出了医药市场,而Lecanemab的长期疗效与安全性还需进一步的证据支持。许多证据表明tau蛋白病理改变与AD病人认知功能损伤的关系更为密切。因此,tau蛋白作为潜在的AD治疗靶标受到了越来越多的关注。同时,神经炎症与tau蛋白在AD整个病理进程中复杂的相互作用也不容小觑。
近日,8188www威尼斯于洋团队在神经免疫知名期刊《Journal of Neuroinflammation》(中科院一区,Top期刊)上发表了题为“Tau and neuroinflammation in Alzheimer’s disease: interplay mechanisms and clinical translation”的综述文章,论述了tau蛋白与神经炎症的相互作用对AD疾病进程的影响,并系统阐述了当前以tau蛋白和神经炎症为靶标的AD新药研发进展,强调了两者在AD新药研发中的潜在临床价值。
Tau蛋白是一种在神经元内表达的可溶性微管结合蛋白,主要功能为参与微管组装、运输营养物质和维持神经元形态等。在AD病理情况下,tau蛋白发生异常的翻译后修饰如过度磷酸化,从微管上解离下来而失去对微管的稳定作用,导致神经元损伤;另一方面,过度磷酸化的tau蛋白能够形成可溶性的寡聚体,并进一步聚集形成不可溶性的神经纤维缠结,这些病理性tau被认为是导致神经毒性的重要原因。在大脑中累积的病理性tau像朊病毒一样具有传染性,如通过神经突触传导、外泌体释放或直接分泌到细胞外,从而被周围正常神经元摄取,导致正常细胞内tau蛋白发生异常聚集并产生病理性tau。靶向tau蛋白的异常翻译后修饰和朊病毒样传播是目前AD新药研发的重要方向。
持续的神经炎症反应被认为是AD的第三大病理特征,并与tau蛋白的病理改变存在紧密联系。参与中枢炎症反应的小胶质细胞及星形胶质细胞可通过各种表面受体(如髓系细胞触发受体2,低密度脂蛋白受体相关蛋白1,CX3C趋化因子受体1,甲酰肽受体2,和趋化因子样受体1等),细胞内炎症相关信号通路(如NLRP3炎症小体,多聚谷氨酰胺结合蛋白1/环GMP-AMP合酶/干扰素刺激因子通路,细胞外信号调节激酶/磷酸肌醇3-激酶通路,和核转录因子NF-κB等),及释放的外泌体或促炎因子(如白介素-1,白介素-6,肿瘤坏死因子-α,血清淀粉样蛋白A,和巨噬细胞游走抑制因子等),间接或直接调节tau蛋白的磷酸化水平和/或病理性tau蛋白的扩散和传播(图1)。尽管适度激活的胶质细胞能够吞噬病理性tau进而缓解AD的病理进展,但持续过度激活的胶质细胞吞噬能力减弱,且通过表面受体吞噬的病理性tau会激活细胞内的炎症相关信号通路,导致病理性tau的释放和传播,tau病理的加剧进一步促进神经炎症反应,二者相互作用导致恶性循环,最终加重AD病理进展。因此,精准调控胶质细胞的免疫功能如增强其吞噬功能,调节表面受体的表达和炎症因子的释放,可能能够通过减少病理性tau及其传播改善AD症状并延缓AD病理进程。
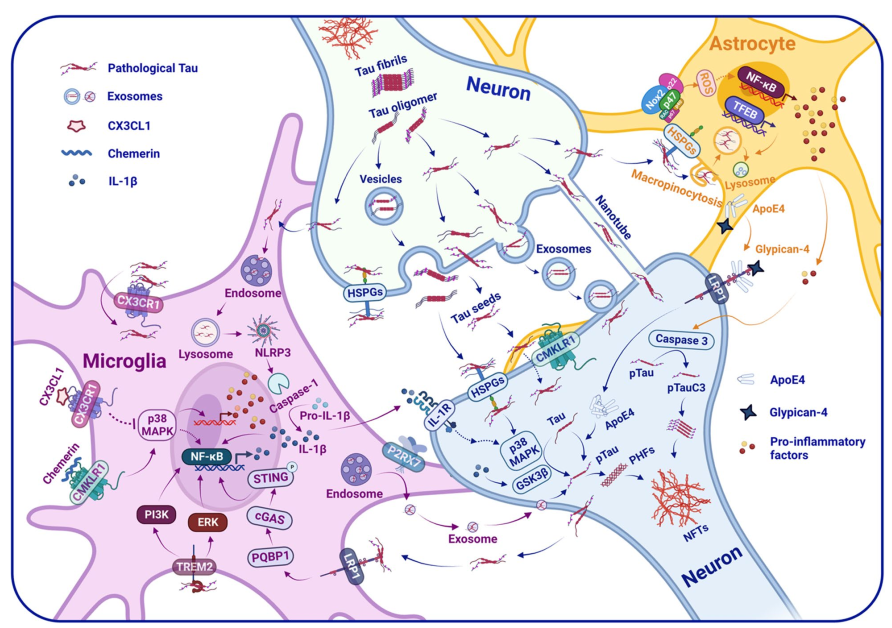
图1. 神经炎症与tau蛋白相互作用示意图(图源: Chen Y, Yu Y., J Neuroinflammation, 2023)
鉴于tau蛋白和神经炎症在AD病理进展中的重要作用,研究人员不断探索以二者为靶标或联合针对这两者的免疫疗法或小分子药物。如下表所示,本篇综述系统总结了目前处于临床试验阶段,靶向tau蛋白和/或神经炎症的代表性AD候选药物(信息采集于美国国立医学图书馆临床试验数据库: Clinicaltrials.gov,及国际知名学术论坛Alzforum:alzforum.org,信息采集截至2023年3月)。
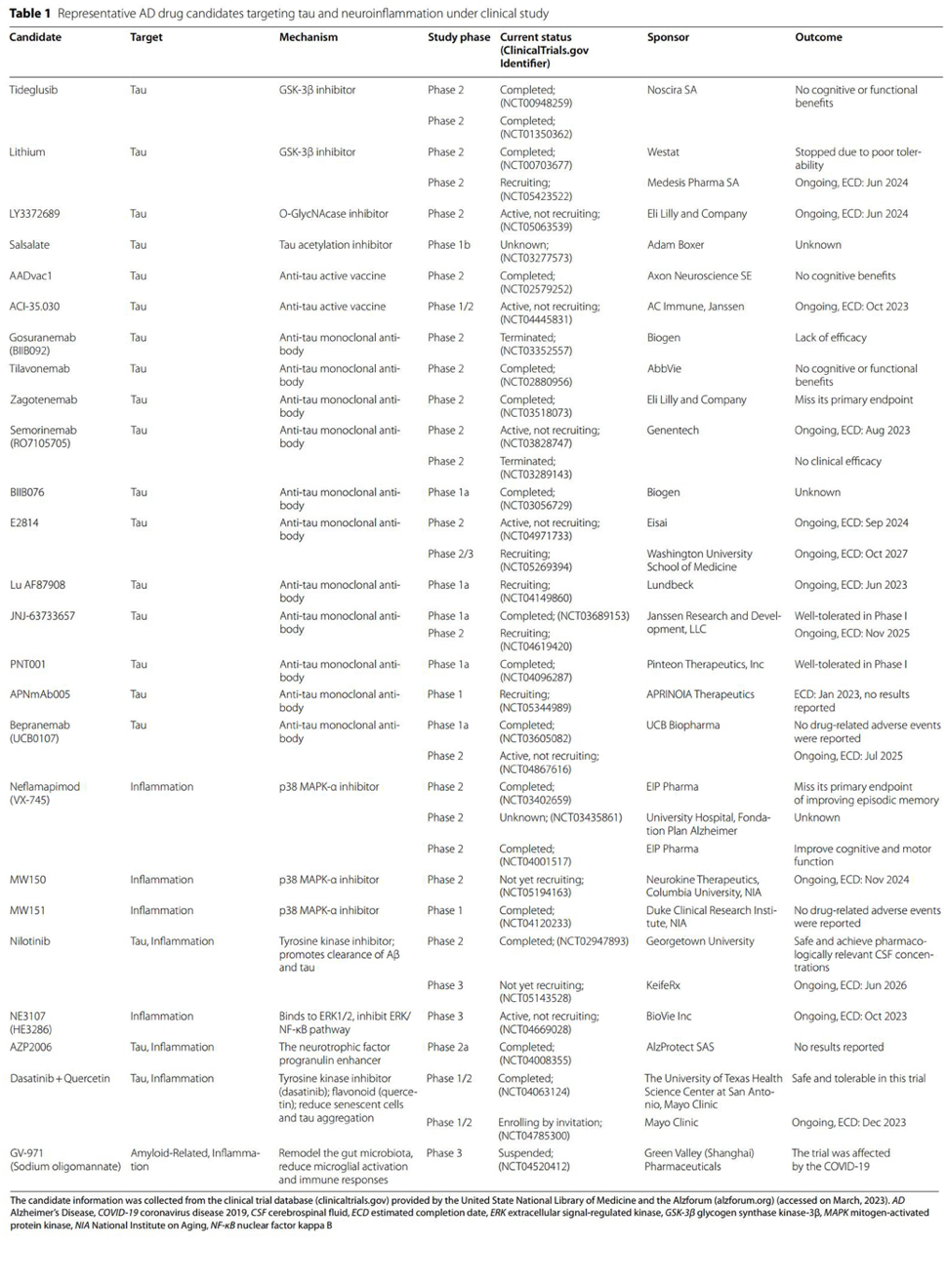
表1. 靶向tau蛋白和神经炎症的AD候选药物(表源: Chen Y, Yu Y., J Neuroinflammation, 2023)
未来阐明神经炎症与tau病理之间精准的时空动态调控将为AD的药物研发提供重要的理论依据。采取针对多靶点(单一药物多靶点或多种药物联合治疗)及精准治疗策略将是未来AD及其它tau蛋白病药物研发的重要方向,并极有可能为这些具有复杂病因疾病的治疗带来实质性的突破。
我院硕士生陈怡君为该文章第一作者,于洋副研究员为通讯作者。该团队一直致力于神经炎症在AD发生发展中的作用及机制研究,该综述为团队前期多项研究成果与该领域其它最新研究成果的全面总结与系统评述。该工作得到了国家及上海市自然科学基金面上项目的支持(81870835,22ZR1434700)。
原文链接:https://jneuroinflammation.biomedcentral.com/articles/10.1186/s12974-023-02853-3
另可参见公众号《逻辑神经科学》2023年8月8日发布的特邀稿:“J Neuroinflammation综述︱上海交通大学于洋团队评述Tau蛋白与神经炎症在阿尔茨海默病中的相互作用及临床应用前景”。